Генеалогический метод изучения закономерностей наследования признаков человека. Методы генетики Генеалогический метод дает возможность изучать природу морфологических
Методы изучения наследственности человека
Цитогенетический метод - изучение хромосомных наборов здоровых и больных людей. Результат изучения - определение количества, формы, строения хромосом, особенности хромосомных наборов обоих полов, а также хромосомных нарушений;
Биохимический метод - изучение изменений в биологических параметрах организма, связанных с изменением генотипа. Результат изучения - определение нарушений в составе крови, в околоплодной жидкости и т. д.;
Близнецовый метод - изучение генотипических и фенотипических особенностей однояйцевых и разнояйцевых близнецов. Результат изучения - определение относительного значения наследственности и окружающей среды в формировании и развитии человеческого организма;
Популяционный метод - изучение частоты встречаемости аллелей и хромосомных нарушений в популяциях человека. Результат изучения - определение распространения мутаций и естественного отбора в популяциях человека.
В основе этого метода лежит составление и анализ родословных. Этот метод широко применяют с древних времен и до наших дней в коневодстве, селекции ценных линий крупного рогатого скота и свиней, при получении чистопородных собак, а также при выведении новых пород пушных животных. Родословные человека составлялись на протяжении многих столетий в отношении царствующих семейств в Европе и Азии.
Как метод изучения генетики человека генеалогический метод стали применять только с начала XX столетия, когда выяснилось, что анализ родословных, в которых прослеживается передача из поколения в поколение какого-то признака (заболевания), может заменить собой фактически неприменимый в отношении человека гибридологический метод.
При составлении родословных исходным является человек - пробанд, родословную которого изучают. Обычно это или больной, или носитель определенного признака, наследование которого необходимо изучить. При составлении родословных таблиц используют условные обозначения, предложенные Г. Юстом в 1931 г. (рис. 6.24). Поколения обозначают римскими цифрами, индивидов в данном поколении - арабскими.
Медицинское значение: С помощью генеалогического метода может быть установлена наследственная обусловленность изучаемого признака, а также тип его наследования (аутосомно-доминантный, аутосомно-рецессивный, X-сцепленный доминантный или рецессивный, Y-сцепленный). При анализе родословных по нескольким признакам может быть выявлен сцепленный характер их наследования, что используют при составлении хромосомных карт. Этот метод позволяет изучать интенсивность мутационного процесса, оценить экспрессивность и пенетрантность аллеля. Он широко используется в медико-генетическом консультировании для прогнозирования потомства. Однако необходимо отметить, что генеалогический анализ существенно осложняется при малодетности семей.
Родословные при аутосомно-доминантном наследовании. (полидактилия)
Родословные при аутосомно-рецессивном наследовании. (ретинобластомой в случае неполной пенетрантности, псевдогипертрофическая прогрессирующая миопатия)


Родословные при рецессивном Х-сцепленном наследовании признаков. (гемофилия, фолликулярный кератоз)


Родословные при Y-сцепленном наследовании. (гипертрихоз ушной раковины)

Гаструляция - сложный процесс морфогенетических изменений, сопровождающийся размножением, ростом, направленным перемещением и дифференцировкой клеток, в результате чего образуются зародышевые листки (эктодерма, мезодерма и энтодерма) - источники зачатков тканей и органов. Второй после дробления этап онтогенеза. При гаструляции происходит перемещение клеточных масс с образованием из бластулы двухслойного или трёхслойного зародыша - гаструлы.
Тип бластулы определяет способ гаструляции.
Зародыш на этой стадии состоит из явно разделенных пластов клеток - зародышевых листков: наружного (эктодерма) и внутреннего (энтодерма).
У многоклеточных животных, кроме кишечнополостных, параллельно с гаструляцией или, как у ланцетника, вслед за ней возникает и третий зародышевый листок - мезодерма, который представляет собой совокупность клеточных элементов, расположенных между эктодермой и эндодермой. Вследствие появления мезодермы зародыш становится трехслойным.
Из эктодермы образуется нервная система, органы чувств, эпителий кожи, эмаль зубов; из энтодермы - эпителий средней кишки, пищеварительные железы, эпителий жабр и легких; из мезодермы - мышечная ткань, соединительная ткань, кровеносная система, почки, половые железы и др.
У разных групп животных одни и те же зародышевые листки дают начало одним и тем же органам и тканям.
Объективное изучение человека, с точки зрения науки, неудобно и достаточно сложно. С чем это связано? Причин достаточно много. Во-первых, человека невозможно "скрещивать" опытным путем, к тому же возраст половозрелости наступает достаточно поздно, хромосомный набор большой, а количество потомков - недостаточное для исследований.
Мир человека
Для того чтобы определить наследственные характеристики того или иного человеческого организма, используется генеалогический метод. С его помощью возможно с высочайшей вероятностью прогнозировать различные заболевания, внешние характеристики, черты характера, передающиеся по наследству.
Наследственный тип всегда связан с определенными признаками передачи генов:

Генеалогический метод имеет в своей основе законы Менделя и впервые был предложен и начал применяться 150 лет назад Ф. Гальтоном. Для того чтобы провести объективное исследование, необходимо наличие сведений о прямых предках и достаточного количества потомков. Составление родословной принято начинать с исследуемого человека - пробанда.
Болезни и человек
Клинико-генеалогический метод использует генетический анализ - достаточно простой и очень информативный прием, для использования которого не требуется дополнительная аппаратура, приспособления и прочее. Более того, его может применять каждый, кто интересуется своей родословной и ответственно относится к планированию собственного потомства.
Медико-патологический семейный фон помогает проанализировать генеалогический метод генетики человека. С вероятно высокой степенью точности он позволяет определить возможное развитие наследственных заболеваний и определить членов семьи, нуждающихся в обследовании. Этим занимается клинико-генеалогический метод. Если данные собраны и обработаны правильно, то вероятность совпадения прогноза врача-генетика с проявлением болезни очень высока.

Некоторые факторы негативно влияют на процесс генетического анализа, например, несчастные случаи или дезориентирование обследуемой группы или отдельных ее членов в социуме. Многие заболевания имеют сильные доминантные признаки и прогнозируются достаточно точно. Это бронхиальная астма, шизофрения, сахарный диабет, врожденные пороки развития, в том числе синдром Дауна. Кроме этого, может быть не сама болезнь, а предрасположенность к ней. Ярким примером являются атопические иммунные состояния, которые определяют высокую чувствительность к некоторым пищевым веществам.
По статистике, в детском возрасте проявляется лишь около 10 % всех наследственных заболеваний, а у пожилых людей этот процент достигает 50. Профилактические меры разрабатываются с учетом среды, в которой находится обследуемый индивид, поскольку она способна кардинально изменить прогноз в ту или иную сторону.
Именно генеалогический метод исследования позволил определить неприемлемость близкородственных браков. Патология в таких семьях настолько ярко проявляется, что детская смертность выше средней в сотни раз. Особенно это утверждение справедливо по отношению к передаче генов по гомозиготному рецессивному аппелю.
Клинико-генеалогический метод широко применяется в прогнозировании и профилактике наследственных психических заболеваний. Значительное место в изучении отводится полярным эндогенным психозам. Характерным примером может быть сочетание непрерывно текущей шизофрении и маниакально-депрессивного синдрома.
Существует множество заболеваний, наследственность которых определена и подтверждена. Встречаются случаи, которые не лечатся даже в условиях современной медицины, так как не до конца изучены.

Крылья бабочки
Буллезный эпидермолиз - очень редкое генетическое заболевание. Характеризуется трудно рубцующимися язвами на коже и слизистых, которые образуются от малейшего прикосновения. Кожа умирает, болезнь переходит на внутренние органы. Лечения не существует.
Каменный гость
Цистиноз характеризуется накапливанием особой аминокислоты - цистина. Причем поражаются в первую очередь кровь, лимфатическая система и почки. Болезнь чаще всего развивается у детей, которые не способны дожить до своего совершеннолетия. Цистиноз вызывает постепенное окаменевание всех органов и систем организма. Исключением является головной мозг, который не поражается совсем. Организм перестает развиваться, замедляются все функции. Лечения не существует.
Пляска святого Витта

Хорея передается по наследству, не связана с полом. Дети страдают в 50 % случаев. Симптомы заболевания характеризуются гротескными мимическими движениями, которые при более низкой амплитуде являются нормальными. Создается впечатление, что больной танцует. Отсюда и название - пляска святого Витта.
Движение в науке
Генеалогический метод использует наука генетика. Изначально он создавался как способ изучить возможности и проблемы наследственности. В настоящее время наука далеко продвинулась вперед. Сегодня возможно, например, исключать мутирующие гены в клетке-носителе, заменяя их здоровыми. Это не носит массового характера, так как изучение и подбор правильного решения - вопросы не одного дня и даже десятилетия.
Собственно, наука в целом, и клинико-генеалогический метод генетики в частности, совершили прорыв в предупреждении многих наследственных заболеваний. Способ основан на использовании генов от трех родителей, то есть клетки остаются родительскими, а меняют лишь генетический материал с носителем больного признака. Однако пока все остается на экспериментальном уровне, в том числе с "поврежденными" человеческими зародышами.

Мы с тобой одной крови
Эритроциты любого человека имеют свои специфические особенности, связанные с системой антитело-антиген. По этим признакам выделяют четыре возможные группы крови. Генеалогический метод используют для прогнозирования наследственной возможности в системе АВ0:
- (0) - I.
- (0А) - II.
- (В0) - III.
- (АВ) - IV.
Огромное значение имеет также наличие или отсутствие в крови человека резус-фактора, который представляет собой белковые фракции на мембранах эритроцитов. Открытие этой особенности позволило прогнозировать его присутствие у плода, когда он находится в утробе матери. Дело в том, что отсутствие резуса у матери и наличие его у ребенка способно вызвать серьезный конфликт, когда организм беременной женщины воспринимает свое дитя как "занозу" и требует его отторжения.

Подарок в День рождения
Генеалогический метод - часть общей системы знаний о человеке. За любые наследственные проявления отвечает 1/10 часть ДНК. Это носитель информации, своего рода человеческий код, программа. Причем, переданы в наследство могут быть не только заболевания, но и специфические особенности внешности и даже характера.
Генеалогический метод выявил множество таких проявлений:
- Патологическое облысение, или алопеция. До сих пор ученые бьются над вопросом о том, какой именно ген или его часть влияют на возникновение этого синдрома. Принято гипотетически считать, что облысение передается при определенной комбинации хромосом у матери и отца.
- Предрасположенность к полноте. По некоторым утверждениям, изменение окружающей человека среды позволило гену, ответственному за выживание, вызывать у своего "хозяина" полноту и даже ожирение.
- Неуравновешенность и злоба. Удивительный факт был открыт короткое время назад. Злость, оказывается, передается по наследству, и чаще от отца к сыну, то есть имеет признак сцепления с полом. Наличие того же гена у девочки может подарить ей патологическую тягу воровать.
- Алкоголизм. Неправильно говорить, что определенная наследственность обеспечивает 100 % наличие недуга, но, по статистике, 50 % им болеют. Основным провоцирующим фактором является окружающая социальная среда.

Вывод по прочитанному
Генеалогический метод используют для сбора анамнеза, построения родословного графика, анализирования, прогнозирования и подбора возможного лечения для пробанда. Роль его в генетических исследованиях велика.
Основные закономерности наследственности, установленные для живых организмов, универсальны и в полной мере справедливы и для человека. Вместе с тем как объект генетических исследований человек имеет свои преимущества и недостатки.
Для людей невозможно планировать искусственные браки. Еще в 1923 г. Н.К. Кольцов отмечал, что "...мы не можем ставить опыты, мы не можем заставить Нежданову выйти замуж за Шаляпина только для того, чтобы посмотреть, какие у них будут дети". Однако эта трудность преодолима благодаря прицельной выборке из большого числа брачных пар тех, которые соответствуют целям данного генетического исследования.
В значительной мере затрудняет возможности генетического анализа человека большое число хромосом - 2п=4б. Однако разработка новейших методов работы с ДНК, метода гибридизации соматических клеток и некоторых других методов устраняют эту трудность.
Из-за небольшого числа потомков (во второй половине XX в. в большинстве семей рождалось по 2-3 ребенка) невозможен анализ расщепления в потомстве одной семьи. Однако в больших популяциях можно выбрать семьи с интересующими исследователя признаками. Кроме того, в некоторых семьях определенные признаки прослежены на протяжении многих поколений. В таких случаях возможен генетический анализ. Еще одна трудность связана с длительностью смены поколений у человека. Одно поколение у человека занимает в среднем 30 лет. И, следовательно, генетик не может наблюдать более одного-двух поколений.
Для человека характерен большой генотипический и фенотипический полиморфизм. Проявление многих признаков и болезней в сильной степени зависят от условий внешней среды. Следует отметить, что понятие "среда" для человека более широкое по сравнению с растениями и животными. Наряду с питанием, климатом и другими абиотическими и биотическими факторами, средой для человека являются и социальные факторы, трудно изменяемые по желанию исследователя. Вместе с тем, человека как генетический объект широко изучают врачи всех специальностей, что нередко помогает установить различные наследственные отклонения.
В настоящее время интерес и внимание к изучению генетики человека активно возрастают. Так, глобальная международная программа " Геном человека" имеет своей задачей изучение генома человека на молекулярном уровне. Для ее решения используются все новейшие современные методы генетики и медицины.
Какими же методами располагает генетика человека в настоящие дни? Их немало: генеалогический, близнецовый, цитогенетический, популяционно-статистический, биохимический, метод генетики соматических клеток и молекулярно-генетический. Рассмотрим подробнее каждый из них.
Относящийся к числу основных в генетике человека, этот метод опирается на генеалогию - учение о родословных. Его сутью является составление родословной и последующий ее анализ. Впервые такой подход был предложен английским ученым Ф. Гальтоном в 1865 г.
Генеалогический метод широко используется для решения как научных, так и прикладных проблем. Он позволяет выявить наследственный характер признака и определить тип наследования. Наряду с этим метод дает возможность установить сцепленное наследование, определить тип взаимодействия генов и пенетрантность аллелей. Генеалогический метод лежит в основе медико-генетического консультирования. Он включает два этапа: составление родословных и их генеалогический анализ.
Составление родословной. Сбор сведений о семье начинается с человека, называемого пробандом. Обычно это больной с изучаемым заболеванием. Дети одной родительской пары называются сибсами (братья-сестры). В большинстве случаев родословная собирается по одному или нескольким признакам. Родословная может быть полной или ограниченной. Чем больше поколений прослежено в родословной, тем она полнее и тем выше шансы на получение полностью достоверных сведений. Сбор генетической информации проводится путем опроса, анкетирования, личного обследования семьи. Опрос начинается обычно с родственников по материнской линии: бабушки и дедушки по материнской линии, с указанием внуков, детей каждого ребенка бабушки и дедушки. В родословную вносят сведения о выкидышах, абортах, мертворожденных, бесплодных браках и др.
При составлении родословной ведется краткая запись данных о каждом члене рода с указанием его родства по отношению к пробанду. Обычно указываются: фамилия, имя и отчество, дата рождения и смерти, возраст, национальность, место жительства семьи, профессия, наличие хронических заболеваний в семье, причину смерти умерших и др.
После сбора сведений составляют графическое изображение родословной, используя систему условных обозначений (рис. 2.1).
Выполняя эту работу, важно соблюдать следующие правила:
1. Составление родословной начинают с пробанда. Братья и сестры располагаются в порядке рождения слева направо, начиная со старшего.
2. Все члены родословной располагаются строго по поколениям в один ряд.
3. Поколения обозначаются римскими цифрами слева от родословной сверху вниз.
4. Арабскими цифрами нумеруется потомство одного поколения (один ряд) слева направо.
5. В связи с тем, что некоторые болезни проявляются в разные периоды жизни, указывается возраст членов семьи.
6. Отмечаются лично обследованные члены родословной.
Графическое изображение родословной может быть вертикально-горизонтальным или расположенным по кругу (в случае обширных данных). Схема родословной сопровождается описанием обозначений под рисунком, которое называется легендой (рис. 2.2).
Генетический анализ родословной
Задача генетического анализа - установление наследственного характера заболевания и типа наследования, выявление гетерозиготных носителей мутантного гена, а так же прогнозирование рождения больных детей в семьях с наследственной патологией.
Анализ родословной включает следующие этапы: 1. Установление, является ли данный признак или заболевание единичным в семье или имеется несколько случаев (семейный характер). Если признак встречается несколько раз в разных поколениях, то можно предполагать, что этот признак имеет наследственную природу. 2. Определение типа наследования признака. Для этого анализируют родословную, учитывая следующие моменты:
1) встречается ли изучаемый признак во всех поколениях и многие ли члены родословной обладают им;
2) одинакова ли его частота у лиц обоих полов и у лиц какого пола он встречается чаще;
3) лицам какого пола передается признак от больного отца и больной матери;
4) есть ли в родословной семьи, в которых у обоих здоровых родителей рождались больные дети, или у обоих больных родителей рождались здоровые дети;
5) какая часть потомства имеет наследуемый признак в семьях, где болен один из родителей.
Аутосомно-доминантное наследование характеризуется тем, что мутантный ген связан с аутосомой и проявляется как в гомозиготном (АЛ), так и в гетерозиготном (Аа) состояниях. В силу этого прослеживаются следующие особенности наследования:
1) передача патологии от больных родителей к детям;
2) оба пола поражаются в равных пропорциях;
3) здоровые члены семьи обычно имеют здоровое потомство;
4) отец и мать одинаково передают мутантный ген дочерям и сыновьям. Возможна передача болезни от отца к сыну.
Клинические проявления болезни могут значительно варьировать в зависимости от экспрессивности и пенетрантности гена. Экспрессивностью называется степень выраженности гена (в нашем случае - тяжесть заболевания). При высокой экспрессивности гена развивается тяжелая, часто с летальным исходом форма заболевания, при низкой - внешне человек здоров. Под пенетрантностю понимается частота проявления мутантного гена среди его носителей. Она определяется отношением числа особей, имеющих данную болезнь (или признак), к числу особей, имеющих данный ген, выраженным в процентах. Например, пенетрантность атеросклероза 40%, синдрома Марфана 30%, ретинобластомы 80% и т.д.
В зависимости от типа наследования общая картина родословной выглядит по-разному
При аутосомно-рецессивиом типе наследования мутанный ген проявляет свое действие только в гомозиготном состоянии По это л причине в гетерозиготном состоянии он может существовать во многих поколениях, не проявляясь фенотипически.
При данном типе наследования заболевание встречаете в родословной редко и не во всех поколениях. Вероятность заболевания у девочек и мальчиков одинакова. Признак может проявиться у детей, родит ели которых были здоровы, но являлось гетерозиготными носителями мутантного гена. Возможны несколько вариантов таких браков:
1) мать аа х отец аа - у таких родителей все дети будут больными (аа);
2) мать Аа х отец аа - 50 % детей будут больными (генотип аа) и 50 % фенотипически здоровыми (генотип Аа), но будут являться гетерозиготными носителями дефектного гена;
3) мать Аа х отец Аа - 25 % детей будут больными (генотип аа), 75 % фенотипически здоровыми (генотипы АА и Аа), но 50 % из них будут носителями мутантного гена (генотип Аа).
Экспрессивность и пенетрантность колеблются в широких пределах (от О до 100%) и сильно зависят от условий внешней среды. По аутосомно-доминантному типу наследуется полидактилия (шестипалость), брахидактилия (короткопалость), ахондроплазия (карликовость), синдром Марфана ("паучьи пальцы") и другие заболевания (рис. 2.3).
При доминантном типе наследования, если один из родителей болен (Аа), вероятность рождения больного ребенка равна 50% при условии полной пенетрантности гена. В случае гетерозиготности обоих родителей (Аа х Аа) больные дети могут родиться с вероятностью 75%. Многие аутосомно-доминантные заболевания в гомозиготном состоянии протекают в более тяжелой форме, чем у гетерозигот. Однако в практике нередки случаи, когда носители доминантного гена остаются фенотипически здоровыми. В результате вид родословной изменяется и появляются пропуски поколений.
Носительство доминантного гена без фенотипического проявления можно заподозрить у одного из родителей, если среди его потомков появились больные с такой же доминантной патологией. Когда у здоровых родителей появился больной ребенок и в родословной есть другие случаи этой болезни, то правомочно предполагать, что у одного из родителей больного был дефектный ген, который не пенетрировал, но был передан потомку.
Доминантный ген может обладать разной степенью экспрессивности, что затрудняет установление аутосомно-доминантного типа наследования. Рассмотрим это на примере наследственной патологии соединительной ткани - синдрома Марфана.
Известно, что частота возникновения наследственных рецессивно-аутосомных болезней находится в прямой зависимости от степени распространенности мутантного гена среди населения. Частота таких болезней особенно повышается в изолятах и среди населения с высоким процентом кровнородственных браков. Такие браки отрицательно влияют на потомство, на это указывает тот факт, что умственная отсталость среди детей от родственных браков в 4 раза выше, чем в семьях с неродственными браками.
При аутосомно-рецессивном типе наследования (как и при аутосомно-доминантном) возможны различная степень экспрессивности и пенетрантности признака. К заболеваниям с аутосомно-рецессивным типом наследования относятся многие болезни обмена веществ, среди которых фенилкетонурия, галактоземия, альбинизм (рис.2.4), муковисцидоз и др. Установлено, что рецессивные заболевания чаще диагностируются в раннем возрасте.
Наследование заболеваний, сцепленных с полом, определяется тем, что мутантный ген расположен в X или Y-хромосоме. Известно, что у женщин имеются две Х-половые хромосомы, а у мужчин - одна Х- и одна Y-хромосома. У человека в Х-хромосоме локализовано более 200 генов. Гены, расположенные в хромосоме X, могут быть рецессивными или доминантными.
У женщин мутантный ген может находиться в обеих Х-хромосомах или только в одной из них; в первом случае она гомозиготна, во втором - гетерозиготна. Мужчины, являясь гемизиготными (имеют только одну хромосому X), передают ее только дочерям и никогда - сыновьям. Любой ген, как доминантный, так и рецессивный, локализованый в его Х-хромосоме, обязательно будет проявляться. В этом главная особенность Х-сцепленного наследования.
Для Х-сцепленного рецессивного наследования характерны следующие особенности:
1) заболевание встречается чаще у лиц мужского пола;
2) от здоровых родителей могут родиться больные дети (если мать гетерозиготна по мутантному гену);
3) больные мужчины не передают заболевание своим сыновьям, но их дочери становятся гетерозиготными носителями болезни;
4) больные женщины могут родиться только в семьях, где отец болен, а мать гетерозиготна по мутантному гену.
Рассмотрим несколько примеров, когда в Х-хромосоме локализован рецессивный ген. Если в брак вступает здоровая женщина и больной мужчина, то в такой семье все дети будут здоровыми, а дочери получат от отца одну Х-хромосому с мутантным геном и будут гетерозиготными носителями (т.к. вторую нормальную Х-хромосому они получат от матери). В том случае, если в брак вступают здоровый мужчина и женщина - носительница патологического гена, то вероятность рождения больного мальчика составит 50% от всех мальчиков и 25% - от всех детей.
Вероятность рождения больных девочек очень низка и возможна лишь, если отец болен, а мать гетерозиготна по мутантному гену. В такой семье половина мальчиков будут больными. Среди девочек болезнь проявится у половины, а другая половина будет нести дефектный ген.
Классическим примером рецессивного, сцепленного с полом наследования, может служить гемофилия. Больные страдают повышенной кровоточивостью. Причина - недостаточное содержание в крови факторов свертывания крови. На рис. 2.5 изображена родословная семьи с гемофилией
Анализ родословной показывает, что болеют только мальчики. (II - 1,4; III - 7,15). Отсюда можно предположить, что ген гемофилии сцеплен с полом. Больные дети чаще рождаются от здоровых родителей и, следовательно, ген болезни рецессивный.
Известно, что гемофилия широко распространена в королевских семьях Европы. Это связано с заключением близкородственных браков. В результате возникшие мутации сохранялись внутри семьи. Королева Виктория в Англии была носительницей гена гемофилии. Ее сын Леопольд родился гемофиликом. Через своих дочерей и внуков королева Виктория передала ген гемофилии Вольдемару и Генриху Прусским, Фридриху Гессенскому, царевичу Алексею Романову, Рупрехту Тех-Атлонскому, двум баттенбергским и двум испанским принцам (рис 2.6). Кроме гемофилии, в Х-хромосоме локализованы рецессивные гены, обусловливающие миопатию Дюшенна, некоторые формы дальтонизма и др. заболевания.
При локализации в хромосоме X доминантного гена тип наследования называется Х-сцепленным доминантным. Для него характерны следующие признаки:
1) болеют как мужчины, так и женщины, однако больных женщин в два раза больше, чем больных мужчин;
2) заболевание прослеживается в каждом поколении;
3) если болен отец, то все его дочери будут больными, а все сыновья здоровыми;
4) если мать больна, то вероятность рождения больного ребенка равна 50 % независимо от пола;
5) больными дети будут только тогда, если болен один из родителей;
6) у здоровых родителей все дети будут здоровы.
По Х-сцеплснному доминантному типу наследуются фосфатемия (недостаток фосфата в крови), коричневая окраска эмали зубов и др.
Имеет свои особенности и Y-сцепленное наследование.
В Y-хромосоме у мужчин локализовано немного генов. Они передаются только сыновьям и никогда дочерям (голандрическое наследование). С Y-хромосомой у мужчин наследуются такие признаки, как гипертрихоз (наличие волос по краю ушных раковин), кожные перепонки между пальцами ног, развитие семенников, интенсивность роста тела, конечностей и зубов. Характерные особенности наследования с Y-хромосомой можно видеть на рис. 2.7.
ЗАКОНОМЕРНОСТИ НАСЛЕДОВАНИЯ ПРИЗНАКОВ ЧЕЛОВЕКА И МЕТОДЫ ИХ ИЗУЧЕНИЯ
ГЕНЕАЛОГИЧЕСКИЙ МЕТОД
При изучении наследования нормальных и патологических признаков человека используют различные методы. Наиболее универсальным является генеалогический, т. е. метод родословных. Его сущность заключается в прослеживании передачи признака (болезни) среди родственников больного в нескольких поколениях. В медицинской генетике метод чаще называют клинико-генеалогическим, поскольку речь идет об изучении патологических признаков в семье с помощью приемов клинического обследования. В отличие от морфологических, иммунологических, биохимических и прочих специальных методов, требующих подчас сложного оборудования и длительного кропотливого лабораторного анализа, клинико-генеалогический метод относительно прост, доступен каждому практическому врачу. В то же время с его помощью можно получить немало полезной информации, что будет способствовать постановке правильного диагноза, а следовательно, назначению адекватного лечения и проведению необходимых профилактических мероприятий. Например, невральная амиотрофия Шарко - Мари и миотоническая дистрофия (наследственные болезни нервно-мышечной системы) имеют сходную клиническую картину (атрофии дистальной группы мышц с последующим парезом). Однако невральная амиотрофия Шарко - Мари наследуется по аутосомно-рецессивному типу, а миотоническая дистрофия - по аутосомно-доминантному. Установление типа наследования является решающим в постановке диагноза, от которого зависит прогноз для больного (болезнь Шарко - Мари приводит к инвалидности в течение 5-6 лет; миотоническая дистрофия течет более доброкачественно и работоспособность сохраняется длительное время), прогноз здоровья потомства этих больных и их лечение.
Одной из основных задач клинико-генеалогического метода является установление наследственного характера болезни. Если в семье встречается один и тот же признак или болезнь несколько раз, то в этом случае можно думать о наследственной природе или семейном характере болезни. Для установления наследственного характера патологии требуется большая тщательность сбора сведений о родственниках больного, полное клиническое и специальное лабораторное и инструментальное обследование определенного круга лиц в родословной (см. ниже). Чтобы не сделать ошибочного заключения о наследственном характере болезни там, где его нет, следует помнить о существовании уже упоминавшихся фенокопий наследственных болезней. Например, микроцефалия в сочетании с умственной отсталостью может явиться следствием редкой моногенной рецессивной мутации. В то же время некоторые препараты, принимаемые матерью во время беременности, или рентгеновское облучение плода могут вызвать аналогичные дефекты и представлять собой фенокопию генетически обусловленного заболевания. Подчас обнаруживаются случаи семейных заболеваний, обусловленных однотипным воздействием различных вредных факторов окружающей среды. "Накопление" болезни в родословной может наблюдаться, например, при семейном характере некоторых профессий. Одни и те же профессиональные вредности могут вызывать сходные заболевания у членов одной семьи. Если исключается действие сходных внешних факторов, можно предположить наследственный характер болезни. После того как обнаружен наследственный характер болезни, клинико-генеалогический метод позволяет установить тип наследования болезни: аутосомно-доминантный, аутосомно-рецессивный, Х-сцепленный доминантный или рецессивный. В случаях таких распространенных заболеваний с наследственной предрасположенностью, как артериальная гипертония, сахарный диабет, язвенная болезнь желудка и другие, с помощью клинико-генеалогического метода можно выявить роль наследственности в происхождении патологии.
Клинико-генеалогический метод имеет большое значение в клинической медицине в плане своевременной диагностики наследственных болезней. Некоторые болезни имеют типичную, легко выявляемую клиническую картину, относительно часто встречаются и поэтому легко диагностируются (например, гемофилия, полидактилия, дальтонизм). Другие наследственные болезни встречаются редко, а для некоторых имеются лишь единичные описания в мировой литературе. Распознать такие болезни практическому врачу трудно. Генеалогический метод дает возможность определить тип наследования болезни и тем самым нередко уточнить ее форму, поскольку для каждой наследственной патологии характерна передача по определенному типу. Особенности передачи наследственных болезней, устанавливаемые с помощью этого метода, позволяют правильно подойти к анализу ранних клинических симптомов, выявляемых у некоторых членов изучаемой семьи, и имеют дифференциально-диагностическое значение. Так, затруднена диагностика основных форм миопатии в начальных стадиях: псевдогипертрофической, ювенильной и плече-лопаточно-лицевой. Изучение генеалогических данных может помочь правильно оценить клинические симптомы болезни, определить ее форму, поскольку для псевдогипертрофической формы характерен сцепленный с полом тип наследования, для ювенильной - аутосомно-доминантный. С этих позиций данные генеалогического метода имеют большое значение для современной диагностики наследственных болезней - до развития выраженных стадий заболевания.
Генеалогический метод дает возможность определить круг лиц в родословной, нуждающихся в детальных исследованиях для выявления гетерозиготного носительства мутантного гена, что особенно важно для медико-генетического консультирования лиц с аутосомно-рецессивными и Х-сцепленными болезнями. Анализ родословной позволяет выявить родственников, нуждающихся в дополнительном обследовании.
В клинической медицине клинико-генеалогический метод служит и основой для изучения гетерогенности (многообразия) наследственных болезней. Принцип генетической гетерогенности состоит в том, что сходные по клиническим данным болезни могут быть вызваны мутациями в разных генах. Примером генетической гетерогенности является врожденная катаракта, которая может быть обусловлена аутосомно-рецессивным, аутосомно-доминантным генами и рецессивным геном, локализованным в хромосоме X. При этом клинические проявления будут совершенно идентичными. Используя клинико-генеалогический метод, можно определить характер наследования в конкретной семье. Генетическая гетерогенность выявлена для многих моногенных болезней.
Генеалогический метод широко используется при медико-генетическом консультировании, в частности для определения прогноза потомства в семьях, где есть или предполагается появление больного с наследственной патологией (см. ниже).
Применение клинико-генеалогического метода в клинической медицине для решения указанных выше вопросов можно рекомендовать в некоторых конкретных ситуациях, когда у больного и его родственников выявляются:
- известное моногенное заболевание;
- болезни с наследственной предрасположенностью (сахарный диабет, гипертоническая болезнь, шизофрения и др.);
- аналогичные заболевания или симптомы у нескольких членов семьи;
- хронические прогрессирующие заболевания неясного происхождения, не поддающиеся обычной терапии. Это может указывать, например, на иммунодефицитные состояния, муковисцидоз и т. д. Так, если у ребенка в раннем детском возрасте развивается острая пневмония, которая затем повторяется, становится затяжной, хронической и не поддается лечению, можно предположить муковисцидоз - наследственную патологию эндокринных желез;
- непереносимость некоторых пищевых продуктов (например, молока при галактоземии, белка злаков при целиакии и т. д.);
- извращенная реакция на действие лекарственных веществ. Например, появление гемолиза эритроцитов при лечении сульфаниламидами может быть вызвано генетически обусловленной недостаточностью глюкозо-6-фосфатдегидрогеназы (Г-6-ФДГ);
- различные аллергические заболевания в семье (например, аллергозы встречаются при некоторых патологиях обмена веществ);
- кровное родство родителей больного ребенка;
- отягощенный акушерский анамнез (бесплодие, выкидыши, мертворождения, ранняя детская смертность, воздействие вредных факторов в период беременности);
- врожденные пороки развития, особенно множественные.
В генеалогическом методе условно можно выделить два этапа: составление родословной и генеалогический анализ.
МЕТОДИКА СОСТАВЛЕНИЯ РОДОСЛОВНОЙ
Сбор генеалогической информации о наличии среди родственников больного тех или иных заболеваний может проводиться разными методами: опрос, очное и заочное анкетирование, личное обследование членов семьи. Основные трудности при применении клинико-генеалогического метода обычно бывают связаны с недостаточным объемом получаемой информации или ее искажением. Это обусловлено тем, что многие люди не знают состояние здоровья и причин смерти даже ближайших родственников и тем более родственников по линии мужа или жены. Естественно, чем больше членов семьи будет непосредственно опрошено, тем выше шансы на получение более достоверных и полных сведений. Необходимо объяснить больному цель тщательного опроса.
Иногда искажение сведений о родственниках жены (мужа) возникает при желании переложить на них "вину" за наследственную болезнь у ребенка. В таких случаях целесообразно опросить каждого из супругов отдельно, соблюдая тайну результатов опроса. Подчас больные сознательно скрывают сведения о наследственных болезнях, особенно таких, как нарушения психики, интеллекта, врожденные пороки развития, а также случаи тяжелых наследственных болезней у детей.
Ограниченность информации, получаемой при сборе сведений со слов, связана с особенностями самого метода, но в значительной степени зависит от умения провести опрос пациентов и установить с ними соответствующий психологический контакт, что особенно важно в работе семейного врача.
Метод анкетирования - второй прием, применяемый для сбора генеалогических данных. Он может дополнять первый или использоваться самостоятельно. Иногда его результаты оказываются более достоверными, чем метода непосредственного опроса пациента. Анкеты заполняют больные, его родственники или лечащий врач. Анкеты содержат различный перечень вопросов в зависимости от целей проводимого обследования. Метод заочного анкетирования применяется в том случае, если родственники больного проживают, например, в другом городе и недоступны для обследования, а получение медицинской информации от них крайне необходимо.
При составлении родословной с целью постановки или же подтверждения диагноза можно использовать выписки из историй болезни, карты новорожденного, протоколы патолого-анатомических исследований.
Молекулярные основы наследственной патологии Ферментопатии Лечение наследственных болезней Заместительная терапия Витаминотерапия Индукция и ингибиция метаболизма Хирургическое лечение Диетотерапия Эффективность лечения мультифакториальных болезней в зависимости от степени наследственного отягощения у больных Разрабатываемые методы лечения Профилактика врожденной патологии у женщин из групп повышенного риска Клиническая фармакогенетика Наследственные дефекты ферментных систем, выявляемые при применении лекарств Атипичные реакции на лекарства при наследственных болезнях обмена веществ Наследственная обусловленность кинетики и метаболизма лекарств Генетические основы тестирования индивидуальной чувствительности к лекарствам Медико-генетическое консультирование Задачи и показания для проведения консультации Принципы консультирования Этапы консультирования Пренатальная диагностика врожденных пороков развития и наследственных болезней Проблемы медико-психологической реабилитации больных с врожденными болезнями и членов их семей Умственная отсталость Дефекты зрения и слуха Аномалии опорно-двигательного аппарата Приложения Блок информации N 1 - ишемическая болезнь сердца Блок информации N 2 - сахарный диабет Блок информации N 3 - язвенная болезнь Блок информации N 4 - врожденные пороки развития на примере расщелины губы и/или неба Литература [показать]
|
У человека как объекта генетического исследования почти нет никаких преимуществ перед другими объектами.
Напротив, много препятствий, затрудняющих изучение его генетики: 1) невозможность произвольного скрещивания в эксперименте; 2) позднее наступление половой зрелости; 3) малое число потомков в каждой семье; 4) невозможность уравнивать условия жизни для потомства; 5) отсутствие точной регистрации проявления наследственных свойств в семьях и отсутствие гомозиготных линий; 6) большое число хромосом; 7) и самым главным затруднением изучения генетики человека в капиталистическом обществе является социальное неравенство, что затрудняет реализацию наследственных потенций человека.
Несмотря на указанные затруднения, генетика разработала некоторые методы, которые позволяют шаг за шагом изучать наследственность и наследование у человека. Существует несколько методов исследования: генеалогический, цитогенетический, близнецовый, онтогенетический и популяционный.
Следует иметь в виду, что любой признак, независимо от того, является ли он признаком дикого типа, т. е. относится к норме, или связан с каким-либо заболеванием, может служить моделью для изучения наследственности. Оградить человека от наследственных болезней или поражения его наследственности так же важно, как и выяснить наследование нормы. В настоящее время генетические методы разработаны главным образом в отношении морфологических признаков, которые генетически определяются достаточно четко (брахидактилия, альбинизм, дальтонизм, пятнистость кожи и волос и т. д.).
Генетическое исследование психических свойств все еще остается проблематичным, так как для них не найдены элементарные критерии признака в генетическом смысле. Почти все признаки Психической и творческой деятельности человека настолько комплексны и сложны, а также в сильной степени обусловлены внешними, в том числе и социальными, факторами, что генетический анализ этих свойств пока трудно осуществим, хотя наследственная их обусловленность не вызывает сомнения.
Можно сказать, что значительное большинство признаков, характеризующих вид Homo sapiens, может изучаться как количественные и сложные физиологические признаки, т. е. признаки, не проявляющие дискретного характера в онтогенезе. Эти признаки контролируются системой генотипа (полигенно). И пока эта система не разгадана хотя бы на примере просто организованных организмов, проблема признаков поведения остается малодоступной для генетического анализа. Напротив, мутантные признаки, выходящие за границы характеристики видовых признаков, служат хорошими генетическими моделями изучения наследственности и наследования в норме.
На дискретные мутантные признаки нельзя смотреть как на признаки только патологические, якобы не имеющие приспособительного значения. Возможно, что само появление человека с развитыми полушариями коры головного мозга, вертикальным положением тела, дискретной речевой сигнализацией является следствием крупных мутаций. В пользу этого свидетельствует очень
короткий промежуток времени эволюции человека, за который мелкие мутации вряд ли могли накопиться в таком количестве и дать такой значительный эволюционный эффект. Разумный человек для природы столь же «необычен», как домашняя курица, несущая 365 яиц в год вместо 10-15, или рекордистка-корова, дающая 16 тыс. кг молока в год вместо 600-700 кг.
Разделение признаков на нормальные и мутантные применительно к человеку и животным необходимо для познания эволюции человека и патологических явлений.
Совокупность видовых признаков человека и животных определяется системой генотипа, сложившейся под влиянием всех факторов отбора в процессе эволюции. Мутации, пребывающие в гетерозиготном состоянии у человека, по-видимому, так же необходимы, как и у животных, для поддержания их в популяции.
Самым опасным в разработке научных методов исследования животных и человека, особенно его способностей, является антропоморфический момент, т. е. выдача желаемого за действительность.
Генеалогический метод
Анализ наследования человека на основе составления родословной - генеалогии был предложен Ф. Гальтоном.
Генеалогический метод представляет собой изучение наследования свойств человека по родословным (педигри). Данный метод применим, если известны прямые родственники - предки обладателя наследственного признака (пробанда) по материнской и отцовской линиям в ряду поколений и имеется достаточное число потомков в каждом поколении, или в том случае, когда имеются данные по достаточному числу разных семей, позволяющему выявить сходство родословных. Данные по совокупности сходных родословных подвергают статистической обработке.
Получившая наибольшее распространение система обозначения родословных человека была предложена Г. Юстом в 1931 г.
На основе большого числа проанализированных семей составляют родословные и производят математические расчеты соответственно типу наследования того или иного признака - доминантному или рецессивному, часто и не часто встречающейся мутации, сцепленному или не сцепленному с полом и т. д. Здесь мы не будем касаться приложения математического метода к данному анализу, отметим только, что весь этот формальный анализ основан на элементарных генетических закономерностях наследования.
Схемы родословной наследования дохминантного аутосомного гена, определяющего какой-либо признак, например заболевание (хондродистрофическая карликовость, буллезный эпидермолиз - свойство кожи образовывать большие пузыри при небольших травмах, ретинобластома и т. д.), или морфологический недостаток, например короткопалость (брахидактилия - отсутствие двух дистальных фаланг в пальцах).

Наследование признаков, определяемых рецессивными генами (рецессивное наследование), анализируется несколько сложнее, при составлении схем родословных.
Например, двоих в семье, появление двоих больных детей равно произведению вероятностей, т. е. 0,25 X 0,25, т. е. 6,25%.

Часто встречающиеся рецессивные аутосомные гены при условии, если носители их (аа) способны вступать в брак и давать потомство, будут находиться в высокой концентрации в популяции. В таком случае становятся очень вероятными браки аа X Аа, в потомстве от которых наследование данного признака будет имитировать наследование по доминантному типу 1:1. Однако, зная тип наследования и проявления тех и других генов даже в случае малочисленных семей, но при достаточном числе таких семей, можно установить истинный характер наследования.
Наследование генов, полностью сцепленных с полом, т. е. находящихся в негомологичных сегментах, и частично сцепленных с полом - локализованных в гомологичных сегментах X- и Y-xpoмосом, подчиняется установленным для половых хромосом закономерностям. Для доминантных и рецессивных генов это наследование будет определяться по-разному в зависимости от того, где данный ген локализован - в гомологичном или негомологичном сегменте X- и Y-хромосомы и каким образом он передается. Так, доминантный ген, вызывающий перепончатость пальцев, находящийся в негомологичном сегменте Y-хромосомы, наследуется от отцов и проявляется только у мужчин.
Для частично сцепленных с полом доминантных генов, находящихся в гомологичных сегментах половых хромосом, анализ несколько более затруднен, но также возможен. Примером сцепленного с полом наследования рецессивного признака является наследование гемофилии. В передаче этого признака в поколениях имеется прерывность; пораженные мужчины являются потомками здоровых матерей, которые были гетерозиготами по данному гену; больные гемофилией женщины могут быть потомками больного отца и больной или здоровой матери.

У человека найдено около 50 сцепленных с полом рецессивных генов. Интересно, что около половины из них обусловливают заболевание глаз. Уже с давних времен было известно, что степень передачи наследственных признаков в родственных (инбридинг) и неродственных браках (аутбридинг) различна. После того, как генетика установила закономерности более частого проявления рецессивных генов при инбридинге, нет необходимости пространно доказывать вред родственных браков. Чем выше коэффициент инбридинга, тем больше вероятность появления наследственных болезней в поколениях. В разных странах среди разных народов и классов общества, а также в разные эпохи родственные браки (между двоюродными, троюродными братьями и сестрами) встречаются с разной частотой. Так, например, в деревнях на островах Фиджи количество родственных браков достигает 29,7%, в некоторых кастах Индии - 12,9, в Японии (Нагасаки) - 5,03, в Голландии - 0,13-0,159, в Португалии- 1,40, в США (Балтимора) - 0,05%, и т. д. Процент родственных браков колеблется в отдельных районах одной и той же страны в зависимости от уклада жизни.
Вредность родственных браков мало заметна в отдельных родословных, но при сравнительном статистическом анализе болезней и смертностей она выступает с полной очевидностью.
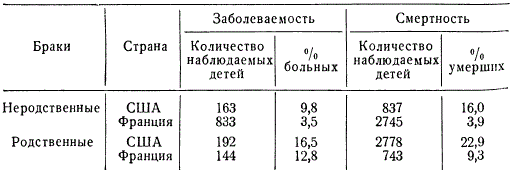
Яркий пример выявления рецессивного гена при родственном браке.
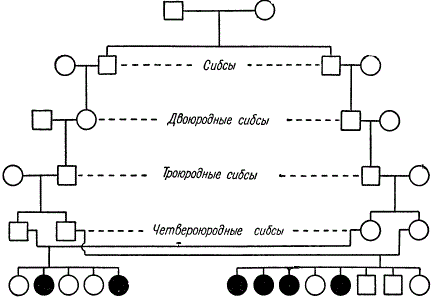
В этой родословной родство поддерживается через бракосочетание сибсов (братья - сестры) разной степени родства. От двух родственных браков (четвероюродные сибсы) появилось в одной семье 4 ребенка из 8, а в другой - 2 из 5, страдающих наследственной амавротической идиотией. К. Штерн предполагает, что один из двух общих предков этих линий передал данный рецессивный ген через три поколения каждому из четырех родителей.
Иногда заболевание и смертность детей от родственных браков превышают на 20-30% таковые от неродственных браков. Очевидно, что причина рассматриваемого явления генетическая, а именно: большая вероятность проявления наследственных заболеваний и смертности в результате гомозиготизации рецессивных генов, определяющих физиологические недостаточности и смертность (летальные и полулетальные гены).
Итак, генеалогический метод является весьма ценным методом, однако его значение в исследованиях тем больше, чем точнее и глубже составлены родословные. По мере роста цивилизации и более точной регистрации родословных роль этого метода в генетике человека будет возрастать.
Близнецовый метод
Близнецами называют потомство, состоящее из одновременно родившихся особей у одноплодных животных (человек, лошадь, крупный рогатый скот, овцы и др.).
Близнецы могут быть однояйцевыми и разнояйцевыми.
Идентичные, или однояйцевые, близнецы (ОБ) развиваются из одного яйца, оплодотворенного одним сперматозоидом, когда из зиготы вместо одного зародыша возникают два или более (полиэмбриония). В силу того, что митотическое деление зиготы дает два равнонаследственных бластомера, однояйцевые близнецы, сколько бы их ни развивалось, должны быть наследственно идентичны и одного пола. Это явление представляет собой пример бесполого, а точнее, вегетативного размножения животных.
Разнояйцевые близнецы (РБ) развиваются из одновременно овулировавших разных яйцеклеток, оплодотворенных разными сперматозоидами. И так как разные яйцеклетки и сперматозоиды могут нести различные комбинации генов, то разнояйцевые близнецы могут быть наследственно столь же разными, как и дети одной и той же супружеской пары, родившиеся в разное время. Разнояйцевые близнецы могут быть одного (РБо) или разного пола (РБр).
Чаще в литературе вместо термина «разнояйцевые близнецы» (РБ) употребляют термин «двуяйцевые близнецы» (ДБ), так как двойни встречаются чаще. Однако термин «разнояйцевые близнецы» лучше подчеркивает разницу между ОБ и РБ; однояйцевые близнецы также чаще рождаются двойнями.
Судя по данным, полученным на млекопитающих, для объяснения образования ОБ у человека может быть несколько гипотез:
- расхождение бластомеров при первом дроблении зиготы и раздельное развитие зародыша из этих бластомеров;
- разделение группы клеток на стадии бластоциста (до гаструляции);
- разделение зародышей на ранней стадии гаструляции. Наиболее вероятным путем предполагают второй.

Число близнецов в одних родах у человека колеблется: чаще всего встречаются двойни, реже тройни, еще реже - четверни, совсем редко - пятерни. По данным И. И. Канаева, за последние 150 лет в США установлено четыре случая родов пятерни, в Канаде - два случая. Факт рождения ОБ - пятерни девочек, доживших до взрослого состояния, - известен в семье канадского фермера Дионн (1934 г.). Рассчитано, что пятерни рождаются один раз на 54 700 816 родов, шестерни - на 4712 млн. родов, семерни известны только как исключение. В среднем частота рождения близнецов составляет 1% с колебаниями в пределах 0,5-1,5%. Близнецы менее жизнеспособные, и поэтому их количество при рождении меньше, чем при зачатии, а во взрослом состоянии меньше, чем при рождении.
Расчет частоты ОБ по отношению к РБ делается исходя из теоретического соотношения однополых и разнополых пар РБ при рождении близнецов: 25%♀♀ + 50%♀♂ + 25%♂♂ вычитание числа пар разного пола из общего числа всех пар одинакового пола (мужского и женского) даст разницу, составляющую число пар ОБ, которая в среднем колеблется от 21 до 33,4% всех близнецов.
Для использования близнецов в генетических исследованиях очень важно точно диагностировать тип ОБ и тип РБ. Диагностика производится на основании следующих критериев:
- ОБ обязательно одного пола, РБ могут быть как одного пола, так и разных полов;
- ОБ имеют, как правило, один общий хорион, РБ - разные хорионы;
- реципрокная трансплантация тканей у ОБ столь же успешна, как и автотрансплантация, у РБ она невозможна;
- наличие сходства (конкордантности) у ОБ и несходства (дискордантности) у РБ по многим признакам.
Для диагностики следует выбирать признаки, четко наследующиеся и менее всего подверженные изменению под влиянием факторов среды; к таким признакам относятся группы крови, пигментация глаз, кожи и волос, кожный рельеф (отпечатки кончиков пальцев, ладоней, ступней и др.). Если по одному-двум таким признакам выявлено различие близнецов, то они, как правило, являются РБ.
Все сомнительные случаи диагностики близнецов могут быть вызваны либо нарушением развития одного из партнеров ОБ, либо сходством родителей по ряду признаков. Однако последнее встречается чрезвычайно редко. Следует заметить, что нарушение развития одного из партнеров ОБ обычно объясняют неодинаковым действием факторов внутриутробной жизни и возникновением соматических мутаций на ранних стадиях эмбрионального развития, до закладки органов. Различного рода генные и хромосомные перестройки, моносомия и другие мутации, возникающие у одного из партнеров, способны вызвать значительные различия в фенотипе ОБ. Поэтому необходимо учитывать возможность соматических мутаций у ОБ в раннем эмбриогенезе.
Согласно обобщениям И. И. Канаева, изложенным в его превосходной монографии сущность близнецового метода в генетике сводится к следующим положениям:
1) пара ОБ имеет тождественную комбинацию, пара РБ - разные комбинации генотипов родителей;
2) для обоих партнеров одной пары ОБ внешняя среда может оказаться одинаковой, а для другой - разной. Если партнеры ОБ в течение жизни испытывают разное влияние, то это приведет к внутрипарному различию. Отсюда пары могут быть с внутрипарной одинаковой и внутрипарной разной средой.
Сравнение ОБ с одинаковой средой с ОБ с разной средой открывает возможность судить о роли влияния среды на внутрипарные различия близнецов в течение всей жизни. Сравнение ОБ с одинаковой средой и РБ с одинаковой средой позволяет выяснить роль наследственного фактора. Такого рода изучение проводят на большой выборке и обрабатывают статистически.
Исходя из разности генетического происхождения ОБ и РБ вытекает, что если по одним и тем же признакам нет различия у ОБ и есть таковые у РБ, то очевидно, что данные различия признаков у последних обусловлены наследственными факторами. Если же внутрипарные различия в тех же признаках встречаются у одного и другого типа близнецов, то очевидно, что они могут быть вызваны факторами среды. Из данных дискордантности у ОБ и РБ по ряду морфологических признаков, видно, что внутрипарное различие у РБ встречается во много раз чаще, чем у ОБ.

Представлены некоторые данные С. Рида относительно сравнительной частоты патологии у второго партнера в случае заболевания одного из близнецов.

В процентах показана частота конкордантности заболеваний у двух типов близнецов, из него видно, что если один партнер заболел одной из указанных болезней, то вероятность заболевания второго у ОБ значительно выше, чем у РБ. В. П. Эфроимсон, анализируя данные по частоте контордантных пар, совершенно правильно указывает, что высокая Наследственная предрасположенность ОБ к заболеваниям проявляется при наличии провоцирующего фактора; без него этот процент будет значительно ниже.
Близнецовый метод дает возможность с наибольшей точностью выяснить наследственную предрасположенность человека к ряду заболеваний и свойств. Другими методами очень трудно или почти невозможно исследовать многие инфекционные и опухолевые заболевания, воспаления кожи и различных органов, а также характеристики нормальной нервной деятельности человека.
При использовании близнецового метода приходится учитывать условия совместного и раздельного воспитания в жизни партнеров, социальные условия, в которых они находятся, и т. д. Тем не менее близнецовый метод позволяет наиболее точно определить, коэффициент наследуемости разных признаков, а также судить о гетерогенности популяции по изучаемым генам и вычленять роль среды в определении изменчивости изучаемых признаков.
Цитогенетический метод
Цитогенетическим методом в генетике человека обычно называют цитологический анализ кариотипа человека в норме и патологии.
Правильнее этот метод называть цитологическим, а не цитогенетическим, поскольку генетический анализ путем скрещивания у человека исключен, и носители хромосомных нарушений если выживают, то оказываются, как правило, бесплодными. Однако изредка в отношении некоторых хромосомных нарушений удается сочетать цитологический метод с генеалогическим и устанавливать связь фенотипического эффекта с определенным типом хромосомных изменений. В силу этих обстоятельств можно сохранить принятый в литературе термин «цитогенетический метод» в изучении генетики человека. В тех же случаях, где такого параллелизма исследовании не ведется, применение данного термина неправомочно.
Цитогенетическим методом исследуют различного рода гетероплоидию и хромосомные перестройки в соматических тканях человека, вызывающие различные фенотипические отклонения от нормы.
Чаще всего этот метод применяют на культуре ткани. Он позволяет учитывать крупные аномалии хромосом, возникающие как в половых, так и соматических клетках. Оказалось, что у человека, так же как и у животных, довольно часто возникают трисомики и моносомики по различным парам хромосом вследствие нерасхождения аутосом и половых хромосом в мейозе. Трисомия и моносомия по половым хромосомам у человека обнаруживаются на основе анализа полового хроматина.
В ходе относительно продолжительного индивидуального развития человека в клетках различных тканей накапливаются аномалии хромосом (хромосомные перестройки, а также изменение числа хромосом). Ткани организма представляют собой разнообразные популяции генетически различающихся клеток, в которых с возрастом концентрация клеток с патологическими ядрами возрастает. В этом случае цитогенетический метод позволяет изучать старение тканей на основе исследования структур клеток в возрастной динамике «популяции» соматических и генеративных тканей.
Поскольку частота возникновения хромосомных аномалий зависит от влияния на организм разнообразных мутагенов (ионизации, химических агентов - фармакологических препаратов, газового состава среды и др.), то цитогенетический метод позволяет устанавливать мутагенное действие факторов внешней среды на человека.
Применение цитогенетического метода особенно расширилось в связи с открытием причин ряда физических и психических заболеваний - так называемых хромосомных болезней.
Существует несколько заболеваний человека, например болезнь Клайнфельтера, Шерешевского-Тернера, Дауна и др., причины которых долго оставались неизвестными, пока цитологическими методами у таких больных не были обнаружены хромосомные аномалии.
Больные мужчины с синдромом Клайнфельтера характеризуются недоразвитием гонад, дегенерацией семенных канальцев, умственной отсталостью, непропорциональным ростом конечностей и т. д. У женщин встречается синдром Шерешевского-Тернера. Он проявляется в замедлении полового созревания, недоразвитии гонад, отсутствии менструаций, бесплодии, малом росте и в других Патологических признаках.
Оказалось, что оба эти синдрома у потомков являются следствием нерасхождения половых хромосом при образовании гамет родителей. Вследствие нерасхождения Х-хромосом у женского гомогаметного) пола в процессе мейоза могут возникать гаметы двумя Х-хромосомами, т. е. XX + 22 аутосомы, и без Х-хромосом, т. е. 0 + 22; у мужского (гетерогаметного) пола соответственно гаметы XY + 22 и 0 + 22. В случае оплодотворения таких яйцеклеток нормальными сперматозоидами (X + 22 или Y + 22) возможно образование следующих классов зигот: XXX + 44, 0Х + 44 и XXY + 44, 0Y + 44.
Из этого следует, что число хромосом у зигот разного происхождения может колебаться от 47 до 45, причем особи 0Y + 44, очевидно, не выживают, так как ни разу не были найдены. Хромосомный набор XXY + 44 присущ мужчине с синдромом Клайнфельтера (мужская интерсексуальность), хромосомные наборы Х0 + 44 и XXX + 44 имеют женщины с синдромом Шерешевского-Тернера.
При дальнейшем анализе больных с разными синдромами выяснилось, что вследствие нерасхождения половых хромосом могут возникать разного типа хромосомные аномалии, в частности полисомия. Встречаются, например, мужчины с такими наборами хромосом: XX Y, XXX Y, ХХХХ Y, а женщины - XXX, ХХХХ.
Особенность роли половых хромосом в детерминации пола у человека в случае их нерасхождения, в отличие от дрозофилы, проявилась в том, что набор хромосом XX Y всегда определяет мужской пол, а набор Х0 - женский. При этом увеличение числа Х-хромосом в сочетании с одной Y-хромосомой не изменяет определение мужского пола, а лишь усиливает синдром Клайнфельтера. Трисомия, или полисомия по Х-хромосоме, у женщин также часто вызывает заболевания, сходные с синдромом Шерешевского-Тернера.
Заболевания, вызванные нарушением нормального числа половых хромосом, диагностируются цитологическим методом - анализом полового хроматина. В тех случаях, когда в тканях мужчин имеется нормальный набор половых хромосом - XY, половой хроматин в клетках не обнаруживается. У нормальных женщин - XX - он обнаруживается в виде одного тельца. При полисомии по Х-хромосомам у женщин и мужчин количество телец полового хроматина всегда на единицу меньше числа Х-хромосом, т. е. n x = n·Х - 1. Так, в клетках мужчин с синдромом Клайнфельтера при наборе XX Y имеется одно тельце полового хроматина, при наборе XXXY - два, при наборе XXXXY - три; у женщин с синдромом Шерешевского-Тернера соответственно: Х0 - нет тельца, XXX - два тельца, ХХХХ - три тельца полового хроматина, и т. д. Предполагается, что в каждой такой зиготе генетически активна лишь одна из Х-хромосом. Остальные хромосомы переходят в гетеропикнотическое состояние в виде полового хроматина.
Причины этой закономерности не выяснены, однако предполагается, что она связана с нивелированием действия генов половых хромосом у гетеро- и гомогаметного пола.
Как мы знаем, нерасхождение хромосом может происходить не только в мейозе, но и в соматических клетках в течение всего эмбриогенеза животного начиная с первых дроблений яйца. В силу последнего среди людей при нарушении расхождения половых хромосом могут появиться больные мозаики-женщины и мозаики-мужчины. Так, например, описаны мозаики следующих типов: двойные: Х0/XX, Х0/XXX и X0/XY, X0/XYY, тройные: Х0/ХХ/ХХХ, XX/X0/XY, а также четверные мозаики, когда соматические клетки одного человека содержат четыре разных набора хромосом.
Кроме рассмотренного типа болезней, вызванных изменением числа половых хромосом в зиготе, хромосомные болезни могут быть вызваны нерасхождением аутосом и разного рода хромосомными перестройками (транслокациями, делециями). Так, например, у детей с врожденной идиотией - болезнью Дауна, сопровождающейся малым ростом, широким круглым лицом, близко расположенным узкими глазными щелями и полуоткрытым ртом, была обнаружена трисомия по 21 хромосоме. Установлено, что частота встречаемости болезни Дауна у новорожденных зависит от возраста матерей.
С врожденными хромосомными аномалиями связывают весьма разнообразные болезни. Поэтому цитогенетический метод приобретает важное значение в этиологии болезней человека.
Популяционный метод
Популяционный метод позволяет изучать распространение отдельных генов или хромосомных аномалий в человеческих популяциях.
Популяционный метод основывается на математических методах. Для анализа генетической структуры популяции необходимо обследовать большую по размеру выборку, которая должна быть репрезентативной - объективно отражать всю генеральную совокупность, т. е. всю популяцию в целом. В обследуемой выборке устанавливают распределение лиц по соответствующим четко очерченным фенотипическим классам, различия между которыми наследственно обусловлены. Затем, исходя из найденных фенотипических частот, определяют генные частоты.
На основе знания генных частот представляется возможность дать описание анализируемой популяции в соответствии с формулой Гарди-Вайнберга и заранее предсказать вероятный характер расщепления в потомстве лиц, относящихся к тем или иным фенотипическим классам. Исследование генных частот имеет важное значение для оценки последствий родственных браков, а также для выяснения генетической истории человеческой популяции в целом.
Частота распространения в популяциях разных аномалий оказывается различной; при этом подавляющее количество соответствующих рецессивных аллелей представлено в гетерозиготном состоянии.

Так, примерно каждый сотый житель Европы гетерозиготен по гену амавротической идиотии (болезнь Шпильмайера-Фогта), тогда как заболевают этой болезнью в юношеском возрасте из 1 млн. только 25 человек, являющихся гомозиготными. Альбиносы в европейских странах встречаются с частотой 1 на 20 000, хотя гетерозиготное состояние этой аллели присуще каждому семидесятому жителю.
Несколько иначе дело обстоит в случае аномалий, наследующихся сцеплено с полом, примером чего может служить дальтонизм - цветная слепота, которая контролируется, по-видимому, рядом аллелей, распределенных по двум тесно сцепленным локусам в Х-хромосоме. Среди мужского населения частота дальтоников (q) соответствует суммарной частоте рецессивных аллелей и составляла, например, в Москве в 30-х годах, по данным Р. И. Серебровской, 7%, в то же время среди женского населения той же популяции цветная слепота была только у 0,5% (q 2), но в гетерозиготном состоянии примерно 13% женщин несут аллели, обусловливающие дальтонизм.
Как мы уже говорили выше, рассматривая генеалогический метод, вероятность появления в потомстве рецессивных гомозигот может быть различной при вступлении в брак лиц, имеющих разную степень родства. Так, у супругов, являющихся по отношению друг к другу двоюродными братьями и сестрами, вероятность рождения детей, гомозиготных по рецессивной аллели, распространенной в популяции с частотой q, составит уже не q 2 , а большую величину, а именно q/16 (1 +15q).
Это связано с тем, что если один из общих предков таких супругов - бабушка или дедушка - нес в гетерозиготе рецессивную аллель, то с вероятностью 1/16 данная аллель передастся обоим двоюродным сибсам.
Вредные последствия родственных браков особенно наглядно проявляются в изолированных популяциях ограниченного размера, так называемых изолятах . Под изолятом понимают группу особей популяции, которые вступают в брак большей частью с особями своей группы и поэтому характеризуются значительным коэффициентом кровного родства. Такими изолятами могут быть отдельные изолированные селения, общины и т. д. Внутри изолята более вероятны родственные браки (инбридинг), и больше шансов на то, что супруги будут нести одинаковые мутантные гены, следствием чего является увеличение вероятности проявления рецессивных аллелей в гомозиготном состоянии. Разные изоляты несут различные концентрации сходных или разных генов.
На Марианских островах и острове Гуам смертность среди местного населения от бокового амиотрофического склероза (связанного с поражением клеток передних рогов спинного мозга) в 100 с лишним раз превышает смертность от этой болезни в других странах. В Южной Панаме в провинции Сан-Блаз весьма заметную часть племени кариба куна составляют альбиносы, которые появляются здесь в каждом поколении. В одном селении на р. Роне в Швейцарии среди 2200 жителей имеется более 50 глухонемых, и еще у 200 обнаруживаются некоторые дефекты слуха. По всей вероятности, во всех подобных случаях резкого увеличения концентрации отдельных аллелей известную роль играет генетический дрифт, неравномерное размножение в прошлом отдельных семей, родов, а также снижение миграции.
По мере роста цивилизации и развития производительных сил общества количество изолятов уменьшается, и их значение для популяции в целом падает. Однако они все еще имеют место.
Знание генных частот, как уже говорилось позволяет предсказывать характер расщепления в потомстве отдельных фенотипических классов родительских особей.
Исходя из формулы Гарди-Вайнберга, можно показать, что при моногенном наследовании расщепление по фенотипу в потомстве доминантных матерей должно осуществляться в соотношении p(1 + pq) доминантов к р рецессивов, или (l+pq):q 2 ; в потомстве рецессивных матерей расщепление по фенотипу должно быть pq 2: q 3 , или p: q.
Приведем пример. В одном исследовании при изучении резус-фактора частота рецессивной аллели rh в популяции составила 0,4, а частота доминантной аллели Rh - 0,6. Отсюда следовало ожидать, что в потомстве резус-положительных матерей частота резус — положительных детей (Rh +) примерно в 7,8 раза будет превышать частоту резус-отрицательных детей (Rh —); в потомстве резус-отрицательных матерей соответствующее превышение будет в 1,5 раза.
Действительные соотношения в обследованной выборке составили:
- в первом случае 1475 Rh + : 182 Rh — , или 8,1: 1,
- во втором случае 204 Rh + : 129 Rh — , или 1,6: 1.
Таким образом, наблюдаемые результаты при расщеплении весьма хорошо соответствуют теоретически ожидаемым результатам, предсказанным на основе анализа генных частот.
Популяционный анализ полиморфизма по группам крови интересен тем, что он помогает понять динамику генетической структуры различных популяций и способствует выявлению связей между ними.
Разные популяции существенно различаются по своей генетической структуре, в частности по группам крови. При этом удается проследить некоторые вполне четкие закономерности. Если концентрация аллели I B наибольшая в районе Индии и Китая, то к востоку и западу от этого района происходит постепенное падение ее вплоть до нуля среди коренных обитателей Америки и Австралии. В то же время у американских индейцев (и аборигенов Австралии и Полинезии) максимума достигает концентрация аллели I 0 . Аллель I А редка у коренного населения Америки, а также в Индии, Аравии, тропической Африке, в Западной Европе.
Для объяснения этих различий в генетической структуре популяций недавно была предложена гипотеза, согласно которой решающим фактором отбора в отношении групп крови системы АВ0 явились эпидемии чумы и оспы. Возбудитель чумы Pasteuvella pest is, обладая свойством антигена 0, оказывается наиболее губительным для людей с группой крови 0, поскольку такие лица не способны вырабатывать достаточное количество антител в случае инфекции. По аналогичной причине вирус оспы наиболее опасен для людей с группой крови А. Там, где свирепствовала чума (Индия, Монголия, Китай, Египет), шла интенсивная элиминация аллели I 0 , а там, где особенно свирепствовала оспа (Америка, Индия, Аравия, тропическая Африка), в первую очередь элиминировалась аллель 1 А. В районах Азии, где чума и оспа были эндемичны, наибольшую частоту получила аллель 1 в.
В главе 5 мы рассмотрели моногенное наследование серповидноклеточной анемии, обусловленное расщеплением по аллелям гена S. Высокая концентрация аллели S в поясе эндемичной малярии (Африка, Средиземноморье) оказалась связанной с повышенной устойчивостью к малярии гетерозигот (Ss) и с возникновением. в результате этого системы сбалансированного наследственного полиморфизма.
Таким образом, в обоих приведенных примерах анализа полиморфизма по группам крови и серповидно-клеточной анемии мы видим, как применение популяционного метода позволяет вскрывать генетическую структуру человеческих популяций.
Онтогенетический метод
Онтогенетический метод позволяет устанавливать по фенотипу носительство рецессивных аллелей в гетерозиготном состоянии и хромосомных перестроек.
Генетической основой проявления рецессивных генов в гетерозиготном состоянии является, по-видимому, неполный блок в цепи синтеза того или иного метаболита, вызванного действием доминантной аллели данного гена.
Известно, что некоторые наследственные болезни проявляются не только у лиц, гомозиготных по аллелям, вызывающим заболевание, но в стертой форме и у гетерозигот. Поэтому в настоящее время усиленно разрабатываются методы определения гетерозиготного носительства в онтогенезе. Так, гетерозиготный носитель фенилкетонурии (повышенное содержание фенилаланина в крови определяется дополнительным введением фенилаланина и последующим определением уровня его (или тирозина) в плазме крови. Наличие гетерозиготности по данной аллели устанавливается по повышенному содержанию фенилаланина. В норме (т. е. у гомозигот по доминантной аллели) уровень фенилаланина не изменяется. В норме в крови присутствует фермент каталаза, необходимый для углеводного обмена, но встречается ген, который в гомозиготном состоянии вызывает отсутствие каталазы. У гомозиготных носителей этого гена наблюдается болезнь акаталаземия - расстройство углеводного обмена. Гетерозиготы занимают промежуточное положение по активности каталазы без большого захождения между доминантными и рецессивными гомозиготами.
По активности каталазы можно точно определить гетерозиготных и гомозиготных носителей аллели акаталаземии среди близких родственников и родителей.
Гетерозиготное носительство аллели, определяющей мышечную дистрофию типа Дюшена, тестируется по активности криатинфосфокиназы. Теперь разработаны, подобные тесты для 40 наследственных болезней, определяемых рецессивными аллелями.
В настоящее время онтогенетический метод обогатился за счет биохимических, иммунологических и молекулярных приемов исследования, описанию которых посвящен ряд специальных руководств.
Важность онтогенетического метода очевидна для установления носительства рецессивного гена в гетерозиготном состоянии у родственников семьи, в которой появляется наследственно больной ребенок. Диагностика в онтогенезе важна для расчета вероятности появления наследственно больных потомков при родственных и смешанных браках. По мере упрощения тестирования гетерозиготного носительства этот метод должен будет внедряться в целях консультации супружеских пар относительно возможности появления заболевания у их детей, а также для изучения распространения мутаций в популяциях.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter .


